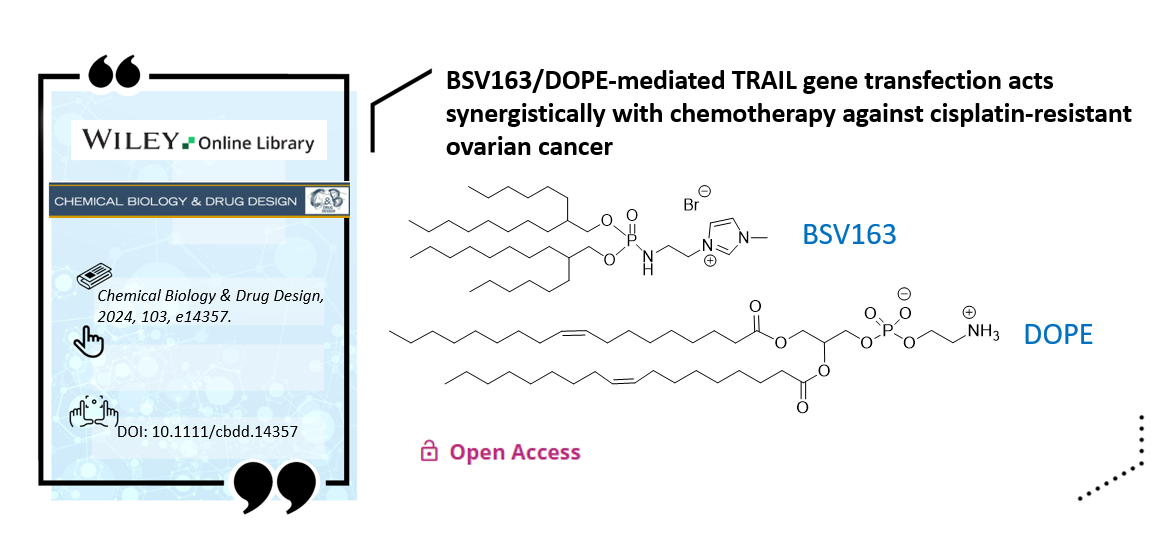
BSV163/DOPE-mediated TRAIL gene transfection acts synergistically with chemotherapy against cisplatin-resistant ovarian cancer
Q.M. Nguyen, P.F. Dupré, M. Berchel, R. Ghanem, P.A. Jaffrès, F. d'Arbonneau, T. Montier
Chem. Biol. Drug Des., 2024, 103, e14357; DOI: 10.1111/cbdd.14357
Le cancer de l'ovaire est le septième cancer le plus fréquemment diagnostiqué chez les femmes dans le monde. La plupart des patientes connaissent des récidives et finissent par succomber à une maladie résistante, ce qui souligne la nécessité d'une option thérapeutique alternative. Nous avons étudié l'effet du gène TRAIL, transfecté par un vecteur lipidique bioinspiré innovant BSV163/DOPE en présence ou en l'absence de cisplatine, pour lutter contre le cancer de l'ovaire sensible et résistant. Nous avons montré que le BSV163/DOPE peut transfecter des lignées cellulaires de cancer de l'ovaire (Caov3, OVCAR3 et notre nouvelle lignée résistante au cisplatine, CR-Caov3) de manière sûre et efficace. En outre, la transfection du gène TRAIL en association avec le cisplatine inhibe plus efficacement la croissance cellulaire (près de 50 % dans les cellules Caov3 après le traitement combiné, et 15 % ou 25 % par chaque traitement seul, respectivement) en raison d'une augmentation du taux d'apoptose, de l'activité des caspases et de l'expression des récepteurs de mort de TRAIL. Plus important encore, cet effet synergique a également été observé dans les cellules CR-Caov3, avec un taux d'apoptose de 35 % après le traitement combiné, contre 17 % après la transfection du gène TRAIL ou 6 % après l'exposition au cisplatine. Ces résultats suggèrent que cette combinaison pourrait avoir une application potentielle pour les patientes atteintes d'un cancer de l'ovaire sensible ou réfractaire.


